Termoquímica
Termoquímica
Ex: fotossíntese (6CO2 + 6H2O + calor -> C6H12O6 + 6O2).
É aquela que libera calor para o ambiente.
Ex: Queima do gás de cozinha (C3H8 + 5O2 -> 3CO2 + 4H2O + calor).
Ex: Queima do gás de cozinha (C3H8 + 5O2 -> 3CO2 + 4H2O + calor).
Representação Gráfica
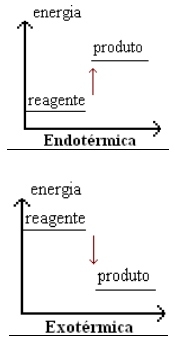
Entalpia (ΔH)
É o conteúdo global de calor de um sistema.
Unidade: Kcal ou KJ (1Kcal ~ 4,18KJ)
A variação da energia de um sistema (ΔH) pode ser calculado pela diferença entre as energias dos produtos e reagentes.
Unidade: Kcal ou KJ (1Kcal ~ 4,18KJ)
A variação da energia de um sistema (ΔH) pode ser calculado pela diferença entre as energias dos produtos e reagentes.
As transformações físicas e as reações químicas quase sempre estão envolvidas em perda ou ganho de calor. O calor é uma das formas de energia mais comum que se conhece.
A Termoquimica é uma parte da Química que faz o estudo das quantidades de calor liberadas ou absorvidas durante as reações químicas. A maioria das reações químicas envolve perda ou ganho de calor (energia).
A Termoquimica é uma parte da Química que faz o estudo das quantidades de calor liberadas ou absorvidas durante as reações químicas. A maioria das reações químicas envolve perda ou ganho de calor (energia).
Veja no quadro abaixo os tipos de reações com perda ou ganho de calor:
REAÇÕES QUE LIBERAM ENERGIA
|
REAÇÕES QUE ABSORVEM ENERGIA
|
Queima do carvão
|
Cozimento de alimentos
|
Queima da vela
|
Fotossíntese das plantas, o sol fornece energia
|
Reação química em uma pilha
|
Pancada violenta inicia a detonação de um explosivo
|
Queima da gasolina no carro
|
Cromagem em para-choque de carro, com energia elétrica
|
As transformações físicas também são acompanhadas de calor, como ocorre na mudanda de estados físicos da matéria.
absorção de calor


SÓLIDO LÍQUIDO GASOSO

liberação de calor
Quando a substância passa do estado físico sólido para liquido e em seguida para gasoso, ocorre absorção de calor.
Quando a substância passa do estado gasoso para líquido e em seguida para sólido, ocorre liberação de calor.
Essa energia que vem das reações químicas é decorrente de rearranjo das ligações químicas dos reagentes transformando-se em produtos. Essa energia armazenada é a ENTALPIA (H). É a energia que vem de dentro da molécula.
Nas reações químicas não é necessário calcular a entalpia. Devemos calcular, geralmente, a variação de entalpia (ΔH).
A variação de entalpia é a diferença entre a entalpia dos produtos e a entalpia dos reagentes.
Quando a substância passa do estado gasoso para líquido e em seguida para sólido, ocorre liberação de calor.
Essa energia que vem das reações químicas é decorrente de rearranjo das ligações químicas dos reagentes transformando-se em produtos. Essa energia armazenada é a ENTALPIA (H). É a energia que vem de dentro da molécula.
Nas reações químicas não é necessário calcular a entalpia. Devemos calcular, geralmente, a variação de entalpia (ΔH).
A variação de entalpia é a diferença entre a entalpia dos produtos e a entalpia dos reagentes.

UNIDADE DE CALOR
Nenhum comentário:
Postar um comentário